Навигация
Производство разбавленной азотной кислоты
5. Производство разбавленной азотной кислоты
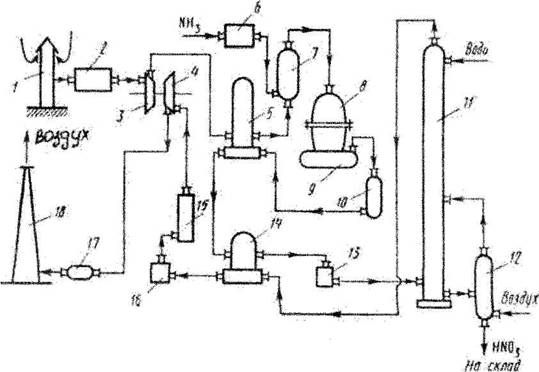
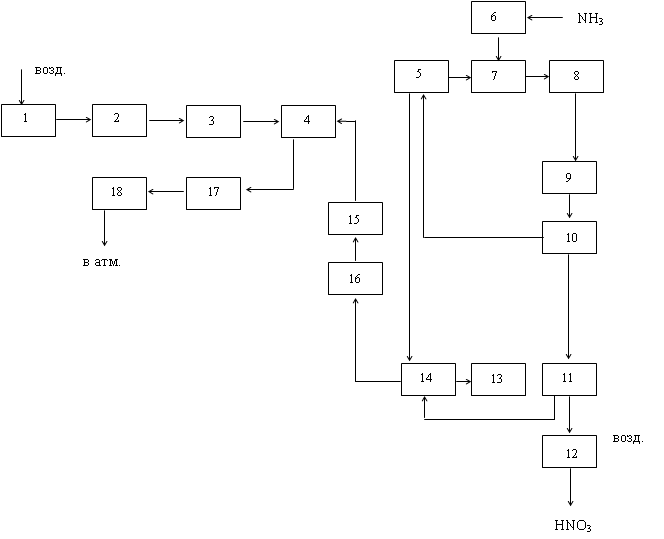
Принципиальная технологическая схема производства разбавленной азотной кислоты под атмосферным давлением представлена на рис. 5.1.
Воздух поступает в систему через заборную трубу, устанавливаемую в местности с чистым воздухом, как правило, вдали от территории завода. Для очистки воздуха от механических и химических примесей устанавливается ситчатый пенный промыватель 1 и картонный фильтр 2. Аммиак, поступающий со склада, также очищается от примесей в картонном фильтре 3. Транспортировка газов через систему осуществляется при помощи аммиачно-воздушного вентилятора 4. Далее газовая смесь проходит в контактный аппарат 5. Горячие нитрозные газы с температурой около 800°С поступают в котел-утилизатор 6, где вырабатывается пар, а температура газов снижается до 250°С. Затем газы охлаждаются водой примерно до 30°С в кожухотрубных холодильниках 7 (на схеме показан один). При этом происходит конденсация водяных паров и в небольшой степени окисление оксида азота до диоксида, который, частично поглощаясь конденсатом, дает разбавленную азотную кислоту.
После этого нитрозные газы газодувкой 8 подаются в абсорбционные башни 9, заполненные насадкой из кислотоупорных колец. Последняя по ходу газа башня орошается водой, а из первой башни отбирается продукционная кислота. Циркуляция кислоты в системе осуществляется насосами 10. Для охлаждения разогретой кислоты, вытекающей из башен, служат водяные холодильники 11. В поглотительных башнях перерабатывается примерно 92% оксидов азота. Кроме того, в процессе абсорбции выделяется NО. Поэтому за абсорбционными башнями устанавливается окислительная башня 12, где происходит частичное окисление NО до диоксида азота. Далее газы поступают в башню 13 (обычно две) для поглощения NО и NО2 раствором соды с образованием так называемых нитрит-нитратных щелоков. Вместо раствора соды можно применять раствор едкого натра или Са(ОН)2. Обезвреженные таким образом выхлопные газы выбрасываются в атмосферу.

Рис. 5.1. Технологическая схема производства азотной кислоты под атмосферным давлением:
1 – пенный промыватель; 2, 3 – картонные фильтры; 4 – аммиачно-воздушный вентилятор; 5 – контактный аппарат; 6 – котел-утилизатор; 7 – кожухотрубный холодильник; 8 – газодувка; 9 – абсорбционные башни; 10 – циркуляционные насосы; 11 – водяной холодильник; 12 – окислительная башня; 13 – санитарная башня.
6. Расчет материального баланса процесса абсорбции нитрозных газов
Данные для расчета
1. Производительность установки – 120 тыс.т/год (на 100 % HNO3).
2. Число рабочих дней в году – 350.
3. Концентрация получаемой кислоты – 50 %(масс.).
4. Общая степень абсорбции NO2 – 92 %.
5. Состав поступающих на абсорбцию газов и концентрация кислоты, подаваемой на орошение абсорбера:
Таблица 6.1
| Состав нитрозных газов, %(об.) | Концентрация кислоты орошающей абсорбер, %(масс.) | ||||
| NO | NO2 | O2 | H2O | N2 | |
| 0,95 | 8,98 | 5,86 | 2,61 | 81,6 | 47,5 |
6. База расчета – суточная производительность установки. Окисление NO в NO2 в абсорбционной башне можно не учитывать.
Расчет суточной производительности установки
![]()
Состав газа в %(масс.):
Для пересчета объемного состава в массовый и обратно необходимо знать плотность ri каждого компонента:
![]()
Масса любого газа при нормальных условиях равна его молярной массе, поделенной на объем, занимаемый одним молем, т.е. ![]() , где
, где ![]() - плотность газа при нормальных условиях.
- плотность газа при нормальных условиях.
![]()
![]()
![]()
![]()
![]()
![]() ;
;
![]()
![]()
![]()
![]()
![]()
Расчет массы двуокиси азота
Абсорбция двуокиси азота происходит по уравнению:
![]()
Концентрация кислоты орошающей абсорбер – 47,5 %(масс.)
Содержание воды и кислоты
![]() - масса кислоты (в пересчете на 100 %-ю) поступающей в абсорбер;
- масса кислоты (в пересчете на 100 %-ю) поступающей в абсорбер;
![]() - масса воды в 47,5 %-ой кислоте.
- масса воды в 47,5 %-ой кислоте.
Рассчитаем количество реагентов для получения 1 кг кислоты (в пересчете на 100 %-ю)
На образование 2-х моль 100% кислоты требуется 3 моль NO2.
![]()
![]()
Масса поглощенной воды на образование 1 кг кислоты (в пересчете на 100 %-ю).
На образование 2-х моль кислоты поглощается 1 моль воды
![]()
![]()
Масса водяных паров, вносимых в абсорбер с нитрозными газами на образование 1 кг кислоты (в пересчете на 100 %-ю).
![]()
![]() ;
;
с учетом степени абсорбции NO2 92 % - ![]() .
.
Для получения 50 %-ой кислоты на 1 кг кислоты требуется 1 кг воды. На разбавление полученной кислоты может использоваться 0,05 кг воды из поступающей на орошение 47,5 %-ой кислоты. Отсюда, количество кислоты подаваемой на орошение составит
0,864/0,05=17,28 кг.
Образуется оксида азота 1 моль
![]()
![]()
Тогда на образование 1 кг азотной кислоты (в пересчете на 100 %-ю) из диоксида азота потребуется:
Нитрозные газы (учетом степени абсорбции):
NO2 – 1,095 кг;
Н2О – 0,136 кг;
Кислота на орошение 17,28 кг.
Образуется оксида азота – 0,238 кг.
Всего получаем кислоты (в пересчете на 100 %-ю):
17,28·0,475+1=9,208 кг или 2·9,208=18,416 кг 50 %-ой кислоты.
17,28 кг кислоты абсорбирует 1,095 кг NO2, тогда 1 кг кислоты абсорбирует Х кг NO2:
![]()
![]() .
.
Поступает с учетом степени абсорбции 92 % - ![]()
Образуется оксида азота:
![]()
![]() .
.
Поглощается воды:
![]()
![]() .
.
Из 0,136 кг воды, содержащейся в нитрозных газах
![]()
![]() .
.
Образуется 100% кислоты при абсорбции 1 кг 47,5 %-ой кислоты:
0,063+0,008 - 0,014 = 0,057 кг
0,057+0,475 = 0,532 кг.
Материальный баланс абсорбера
Таблица 6.2.
| № п/п | Приход | кг | т/сут | № п/п | Расход | кг | т/сут |
| 1 | Азотная кислота 47,5% | 1 | 644,46 | 1 | Азотная кислота 50 % | 1,064 | 685,71 |
| в том числе: | в том числе: | ||||||
| HNO3 | 0,475 | 306,12 | HNO3 | 0,532 | 342,86 | ||
| H2O | 0,525 | 338,34 | H2O | 0,532 | 342,86 | ||
| 2 | Нитрозные газы | 0,495 | 297,12 | ||||
| в том числе: | 2 | NO | 0,019 | 12,49 | |||
| NO2 | 0,069 | 45,85 | 3 | N2 | 0,382 | 224,60 | |
| H2O | 0,008 | 5,05 | 4 | O2 | 0,031 | 18,43 | |
| NO | 0,005 | 3,19 | 5 | NO2 | 0,006 | 3,99 | |
| N2 | 0,382 | 224,60 | |||||
| O2 | 0,031 | 18,43 | |||||
| ИТОГО: | 1,495 | 941,58 | ИТОГО: | 1,502 | 945,21 |
Расхождение баланса составляет:
![]() , что вполне допустимо.
, что вполне допустимо.
ЛИТЕРАТУРА
1. Паушкин Я.М., Адельсон С.В., Вишнякова Т.П. Технология нефтехимического синтеза, в двух частях. Ч. I. Углеводородное сырье и продукты его окисления. М.: «Химия», 1973. – 448 с.
2. Кутепов А.М., Бондарева Т.И., Беренгартен М.Г. Общая химическая технология. Учебник для технических ВУЗов. – М.: «Высшая школа», 1990. – 512 с.
3. Основы химической технологии: Учебник для студентов вузов / Под ред. Мухленова И.П. – М.: «Высшая школа», 1983. – 335 с.
4. Соколов Р.С. Химическая технология: Учеб. пособие для студ. высш. учеб. заведений: В 2 т. – М.: Гуманит. изд. центр БЛАДОС, 2000. – Т.1: Химическое производство в антропогенной деятельности. Основные вопросы химической технологии. Производство неорганических веществ. – 368 с.
Похожие работы
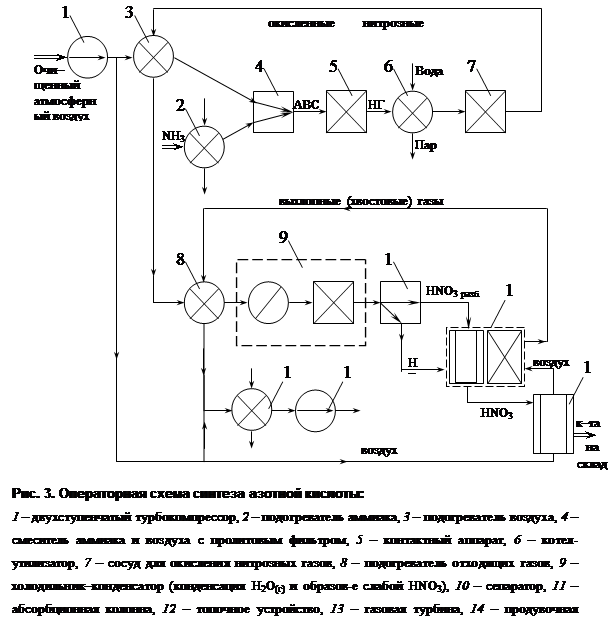
... + 50 2 = 4NO + 6Н2О 2NO+O2=2NO2 3NO2 + H2O = 2NО3 + N0 NH3 + 2О2 = HNO3 + Н2О + 421,2 Технологическая схема Рис. 3. Технологическая схема производства азотной кислоты 1-воздухозаборная труба; 2-воздухоочиститель; 3-газовый компрессор; 4-газовая турбина; 5-воздухоподогреватель; 6-испаритель аммиака; 7-смеситель с фильтром; 8-контактный аппарат; 9,17-котёл-утилизатор; 10-окислитель с ...
... в производстве концентрированной азотной кислоты по методу прямого синтеза. В отдельных случаях используется для обогащения АВС при получении неконцентрированной азотной кислоты. СОВРЕМЕННОЕ СОСТОЯНИЕ ТЕХНОЛОГИИ ПРОИЗВОДСТВА НЕКОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ. Азотная кислота и главным образом ее природная соль - натриевая селитра известны с давних времен. В 778 г. Арабский ученый Гебер ...
... очистки выхлопных газов, выпускающий продукцию в виде 53–58% -ной HNO3. Технологическая схема этого производства в упрощенном варианте представлена на рисунке 5. Подготовка сырья Рис.5 Схема производства азотной кислоты под давлением 0,716 МПа с приводом компрессора от газовой турбины: 1 – фильтр воздуха; 2 – реактор каталитической очистки; 3 – топочное устройство; 4 – ...
... способствует образованию NO2. При температурах до 100 ºС равновесие реакции практически полностью сдвинуто в правую сторону. Окисление диоксида азота – самая медленная стадия получения азотной кислоты. Она сильно зависит от концентрации реагентов, давления температуры. Применение воздуха, обогащенного кислородом (или чистого кислорода) позволяет получать НГ[2] с повышенным содержанием ...



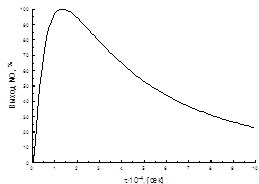



0 комментариев