Навигация
ФИЗИКО-ХИМИЧЕСКАЯ ХАРАКТЕРИСТИКА ПРОЦЕССА
1. ФИЗИКО-ХИМИЧЕСКАЯ ХАРАКТЕРИСТИКА ПРОЦЕССА
1.1МЕТОДЫ ПРОИЗВОДСТВА ГОТОВОГО ПРОДУКТА И ИХ КРАТКАЯ ХАРАКТЕРИСТИКА. ВЫБОР МЕТОДА, ЕГО ПРЕИМУЩЕСТВА
Существует 3 метода производства поливинилбутираля: в спиртовом растворе, из полвинилацетата с применением не смешивающихся с водой растворителей, из поливинилового спирта и масляного альдегида. Реакция образования поливинилацеталей впервые была описана учёными Германом и Генелем в 1927 году. При определённых условиях поливинилацетали образуются почти со всеми альдегидами – алифатическими, ароматическими, предельными и непредельными. Однако в промышленности нашли применения не многие: поливинилформаль, поливенилэтиналь, поливенилбутираль. Основная масса поливинилбутираля производится конденсацией поливинилового спирта с масляным альдегидом. Этот метод самый простой и доступный. Метод осуществляется периодически, что позволяет проводить ремонт оборудования.
1.1.1 Получение поливинилбутираля в спиртовом растворе
Весь процесс проводится в реакционном котле без отделений промежуточных продуктов. В качестве сырья применяют винилацетат, метиловый спирт СН3ОН или этиловый спирт С2Н5ОН, перекись бензоила (инициатор), концентрированную серную кислоту H2SО4 (катализатор), масляный альдегид, едкий натр NaOH. Конечный продукт окрашен в жёлтый цвет и имеет ограниченное применение.
Достоинства: доступность сырья.
Недостатки: продукт получается окрашенный, многостадийный процесс
1.1.2 Получение поливинилбутираля из поливинилацетата с применением несмешивающихся с водой растворителей
Одновременно осуществляется гидролиз поливинилацетата и ацеталирование образовавшегося поливинилового спирта. Удаление несмешивающихся с водой растворителей из реакционной смеси (при выделении поливинилового спирта) значительно упрощается. В некоторых случаях процесс одновременного омыления и ацеталирования осуществляется в отсутствии органических растворителей в водной эмульсии. Применение растворителей, смешивающихся с водой, влечёт за собой экономически невыгодные операции осаждения поливинилбутираля и регенерации растворителей.
Достоинства: доступность сырья, образование поливинилового спирта в одну стадию.
Недостатки: экономически невыгодная стадия осаждения поливинилбутираля и регенерации растворителей.
1.1.3 Получение поливинилбутираля из изолированного поливинилового спирта
Поливинилацетат предварительно гидролизуется и полученный поливиниловый спирт выделяется. Уже после этого поливиниловый спирт подвергается обработке масляным альдегидом в присутствии катализатора – НСl. В качестве растворителя применяется обессоленная вода. Получаемый поливинилбутираль нерастворим в воде и выпадает из раствора в осадок. Выделение поливинилбутираля сводится к отфильтровыванию и отмывке кислоты.
Достоинства: получаемый продукт более высокой степени чистоты. Так как метод периодический, он позволяет проводить ремонт какого-либо оборудования, не останавливая всего процесса производства, доступный растворитель.
Недостатки: образуется много побочных веществ.
1.2ОСНОВНЫЕ ФИЗИКО–ХИМИЧЕСКИЕ СВОЙСТВА СЫРЬЯ, ПОЛУПРОДУКТОВ И ГОТОВОЙ ПРОДУКЦИИ. ХАРАКТЕРИСТИКА ИХ КАЧЕСТВА СОГЛАСНО СТАНДАРТАМ
Для производства поливинилбутираля применяют: 10% водный раствор поливинилового спирта, гидроксид натрия, соляная кислота, масляный альдегид.
1.2.1Поливиниловый спирт
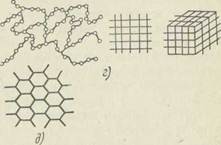
Поливиниловый спирт – порошок от белого до кремового цвета, растворимый в воде и стойкий к действию жиров и масел, кетонов, простых и сложных эфиров, алифатических, ароматических и хлорированных углеводородов. Свойства поливинилового спирта зависят от молекулярной массы и содержания неомылённых ацетатных групп. Поливиниловый спирт – кристаллический полимер с изотактической или синдиотактической структурой:
Показатели основных свойств поливинилового спирта приведены ниже:
Плотность, кг/м3...........................................................1200 – 1300
Разрушающее напряжение, МПа
при растяжении.......................................................98,1–137,2
при статическом изгибе..........................................58,9 – 63,8
Относительное удлинение при разрыве, %.........................3 – 5
Модуль упругости при изгибе, МПа........................ ...........5300
Теплоёмкость по воде, °С.............................................150 – 160
Температура стеклования, °С...................................................85
Растворимость в горячей воде, %.............................................99
Удельная вязкость, кДж/моль..............................................4 – 6
Наибольшее распространение получил синтез поливинилового спирта щелочным омылением поливинилацетата в безводном спирте. Процесс протекает по схеме:
![]()
![]() Кислотное омыление полвинилацетата водят в среде этанола, где кислота является только катализатором:
Кислотное омыление полвинилацетата водят в среде этанола, где кислота является только катализатором:
Растворимость поливинилового спирта зависит от содержания ацетатных групп. При 5 – 10% содержание ацетатных групп поливиниловый спирт хорошо растворяется в воде.
Технические требования на раствор поливинилового спирта: содержание ацетатных групп не более 3%
сухой остаток для поливинилбутираля
лакового «А», не менее 8%
для остальных, не менее 10%
содержание летучих, не более 2%
Поливиниловый спирт не токсичен.
1.2.2Гидроксид натрия. Физические свойства
Гидроксид натрия, формула – NaOH (м = 40,00 г/моль) – белое непрозрачное очень гигроскопичное вещество. Температура плавления 320°С; температура кипения 1378°С; плотность 2,13 г/см; растворимость в воде 107 г/100 г (20°С). Не горюч. При соприкосновение с водой выделяется большое количество тепла.
Химические свойства:
Гидроксид натрия поглощает диоксид углерода из воздуха с образованием карбоната натрия:
2NaOH + C02![]() Na2C03 + H20
Na2C03 + H20
Хорошо растворяет жиры, превращая их в глицерин и мыла - соли органических кислот. Гидроксид натрия является сильным основанием, взаимодействует с кислотами, с кислотными и аморфными оксидами:
NaOH + НС1 ![]() NaCl + Н20
NaCl + Н20
2NaOH + ZnO + Н20 ![]() Na2[Zn(OH)4]
Na2[Zn(OH)4]
Ввиду сильного разъедающего действия на ткани, кожу, бумагу и другие органические вещества гидроксид натрия называют едким натром:
СН3ОН + NaOH ![]() CH3ONa + Н2О
CH3ONa + Н2О
1.2.3Соляная кислота. Физические свойства:
Соляная кислота, формула НСl (м = 36,5 г/моль) – в чистом виде соляная кислота представляет собой бесцветную жидкость с резким запахом. Техническая кислота окрашена примесями (солями железа) в жёлтый цвет. Соляная кислота хорошо растворима в воде. Кислота химически активная, плотность 1,19 г/см и содержит около 37% НСl.
Химические свойства: Хлорид водорода соединение прочное, начинает разлагаться на водород Н2 и С12 лишь при температуре выше 1000°С. При реакции нейтрализации из кислоты и щёлочи получается соль и вода:
NaOH + НС1 ![]() NaCl + Н2О
NaCl + Н2О
2NaOH + H2S04![]() Na2SО4 + H2О
Na2SО4 + H2О
2NaOH + Cl2![]() NaClO + NaCl + H2O
NaClO + NaCl + H2O
Взаимодействует с металлами:
2HCl+Zn ![]() ZnCl2 + H2
ZnCl2 + H2
1.2.4Масляный альдегид:
Встречается в воздухе цехов химических, резиновых, лакокрасочных пластмассовых, текстильных и других производств; содержится в прогорклом масле, в масле зеленого чайного листа, эвкалипта, табака. Применяется в производстве поливинилбутираля (бутвара) и масло–спирто–растворимых смол.
Получается каталитическим окислением бутилового спирта; гидрированием кротонового альдегида в присутствии платиновой черни или никеля.
Масляный альдегид. Физические свойства:
Масляный альдегид, формула СН3СН2СН2СНО (м = 72,1 г/моль) – бесцветная жидкость с острым запахом. Температура кипения 74,8 – 75,7 °С; температура плавления – (–97,1 °С); плотность – 0,817 г/см3.
Масляный альдегид ГОСТ ТУ 6–09–3828–74 утерян.
1.2.5Деминерализованная вода. Физические свойства
Деминерализованная вода, формула – Н20 (м = 18 г/моль) – простейшее устойчивое соединение водорода с кислородом, жидкость без запаха, вкуса и цвета. Некоторые параметры, характеризующие свойства воды при атмосферном давлении:
Температура кипения, °С ...................................................100
Температура плавления, °С.................................................0
Температура критическая, °С.............................................374,15
Давление критическое, МПа..............................................22,06
Плотность жидкости при 20ºС, г/см3................................0,998
Теплопроводность, МВт/(м•К):
жидкости при 273 К.............................................................561
жидкости при 318 К.............................................................645
Диэлектрическая проницаемость:
жидкости при 25°С.............................................................78,3
Показатель преломления:
жидкости при 20°С.............................................................1,3333
пара при 0°С и 0,1 МПа......................................................1,000252
Температурный коэффициент объёмного расширения, °С:
жидкости при 0ºС..............................................................–3,4 • 10–5
жидкости при 10°С............................................................9 • 10–5
жидкости при 20°С............................................................2,0 • 10–5
Плавление льда при атмосферном давлении сопровождается уменьшением объёма на 9%. Температурный коэффициент объёмного расширения льда и жидкой воды отрицателен при температурах соответственно ниже –210°С и 3,98°С. Теплоёмкость Ср° при плавлении возрастает почти в двое и в интервале 0 – 100°С почти не зависит от температуры (имеется минимум при температуре 35°С). Минимум изотермической сжимаемости 144,9 • 10–11 Па–1, наблюдаемый при 46°С, выражен довольно чётко. При низких давлениях и температурах до 30°С вязкость воды с ростом давления падает. Высокая диэлектрическая проницаемость и дипольный момент воды определяют её хорошую растворяющую способность по отношению к полярным и ионогенным веществам.
Химические свойства:
При обычных условиях с водой взаимодействует до половины растворённого в ней хлора и значительно меньше количества брома и йода. При повышенных температурах хлор и бром разлагают воду с образованием водорода и кислорода. При проникновении паров воды через раскалённый уголь она разлагается и образуется так называемый водяной газ:
Н2О + С ![]() СО + Н2
СО + Н2
При повышенной температуре в присутствии катализатора вода реагирует с СО, СН4 другими углеводородами, например:
Н2О + СН4![]() СО + 3Н2 (катализатор Ni или Сo)
СО + 3Н2 (катализатор Ni или Сo)
Эти реакции используют для промышленного получения водорода. Фосфор при нагревании с водой под давлением в присутствии катализатора окисляется в метафосфорную кислоту.
Вода взаимодействует со многими металлами с образованием водорода и соответствующего гидроксида, со щелочными и щелочноземельными металлами (кроме магния). Эта реакция протекает уже при комнатной температуре:
2Na + 2H2О![]() 2NaOH + H2
2NaOH + H2
1.2.6Поливинилбутираль. Физические свойства
Поливинилбутираль, формула СНзСН2СН2СНО (М = 72,10 г/моль) – является продуктом ацеталирования поливинилового спирта. Поливинилбутираль представляет собой ацеталь, содержащий бутиральные, гидроксильные и ацетатные группы. Имеет следующую эмпирическую формулу:
CH3 XУ Z
где:
1) х: 71,0–77,45 массовых %;
у: до 4,35 массовых %;
z: 100 – (х + у) массовых %;
2) для лакового поливинилбутираля марки «А»:
х: 64,54–72,61 массовых %;
у: до 4,35 массовых %;
z: 100 – (x + у) массовых %
Поливинилбутираль – белый горючий порошок. Хорошо растворим в сложных эфирах, в метиловом, этиловом, пропиловом спиртах, циклогексаноне и хлорированных углеводородах. Нерастворим в углеводородах парафинового ряда. Поливинилбутираль обладает хорошей стойкостью к испарению, высокой атмосферостойкостью, стойкостью к действию солнечных лучей. Имеет высокую термостойкость – разлагается при нагревании до 160°С и выше. Поливинилбутираль содержит 78% бутиральных и 2 – 3 ацетатных групп. Обладает хорошими адгезионными свойствами.
Похожие работы
... и окиси тетрафторэтилена посредством конденсации фторсодержащих веществ в ловушках при -120 °С и атмосферном давлении с последующей низкотемпературной ректификацией [5]. 1.4 Обезвреживание газовых выбросов в производстве поливинилхлорида Винилхлорид поступает в атмосферу при вскрытии и чистке полимеризаторов и другого емкостного оборудования, при выделении ПВХ из суспензии в процессе ...
... ), капролактам (ГОСТ 7850-86), лапрол (ТУ 2226-023-104880-57-95). Основное содержание экспериментальной части Глава 3. Физико-химические основы технологии поликонденсационного наполнения базальто-, стекло- и углепластиков Сущность процесса поликонденсационного наполнения заключается в том, что для формирования полимерной матрицы пропитка нитей осуществляется не ФФС (традиционный способ), а ...
... с фенольными полимерами поливинилбутираль используют для приготовления универсальных клеев, например широко известного марки БФ. Глава 2. МЕТОДЫ ОЧИСТКИ СТОЧНЫХ ВОД, СОДЕРЖАЩИХ ОТХОДЫ ПОЛИВИНИЛОВОГО СПИРТА переработка отход поливиниловый спирт Сточные воды ряда производств поливинилацетатных пластмасс (суспензионного ПВА, ПВАД, сополимерных дисперсий ВА с этиленом — СВЭД и дибутилмалеинатом ...
... , водостойкость удовлетворительная. Более теплостоек клей ВС-10Т, который отличается высокими характеристиками длительной прочности, выносливости и термостабильности при склеивании металлов и теплостойких неметаллических материалов. Фенолокремнийорганические клеи содержат в качестве наполнителей асбест, алюминиевый порошок и др. Клеи являются термостойкими, они устойчивы к воде и тропическому ...




0 комментариев