Навигация
3. Исходный уровень знаний
Для выполнения лабораторной работы студент должен знать:
1) правила работы в химической лаборатории;
2) химические и физические свойства используемых соединений;
3) понятие о концентрации растворов: процентная (массовая доля), молярная, нормальность;
4) определение грамм-эквивалента вещества для различных соединений: кислот, солей, оснований;
5) метод кислотно-основного титрования, метод весового анализа, правила приготовления растворов, фильтрование (простое и под вакуумом), способы определения плотности растворов;
6) закон эквивалентов и методы расчета концентрации раствора и содержание вещества;
7) понятие о гетерогенных системах.
Для выполнения лабораторной работы студент должен уметь:
1) правильно пользоваться химической посудой и лабораторным оборудованием;
2) взвешивать необходимое количество вещества;
3) приготавливать растворы требуемой концентрации;
4) проводить титрование и фильтрование.
4. Цель самоподготовки
Для проведения лабораторной работы «Каустификация содового раствора» студент должен самостоятельно изучить следующие вопросы:
1) правила техники безопасности при выполнении данной работы;
2) теоретические основы производства гидроксида натрия известковым методом;
3) влияние температуры и соотношения исходных реагентов в загрузке на равновесную степень каустификации;
4) методику выполнения лабораторной работы;
5) методы обработки экспериментальных данных.
5. Инструкция по технике безопасности
В лабораторной работе используются вредные вещества: гидроксид натрия, оксид кальция, карбонат натрия. Водные растворы этих веществ имеют щелочные свойства. Все сильные основания при высоких концентрациях вызывают тяжелые ожоги кожи и слизистых оболочек. /3, 4, 8/.
Первая помощь при ожогах кислотами и щелочамиВ лабораторной работе «Каустификация содового раствора» используются вредные вещества: гидроксид натрия, оксид кальция, карбонат натрия, соляная кислота. Все сильные основания и кислоты при высоких концентрация вызывают тяжелые ожоги кожи и слизистых оболочек.
При проливе крепких кислот или растворов сильных щелочей необходимо немедленно отключить все нагревательные приборы, пролитый продукт засыпать песком или собрать тряпкой, песок (тряпку) удалить из лаборатории, рабочее место промыть водой после чего дополнительно обработать слабым раствором щелочи (кислоты) соответственно и снова – водой. В случае необходимости проветрить комнату.
При ожоге гидроксидом натрия необходимо хорошо и обильно промыть пораженное место проточной водой, затем 2 % - ным раствором уксусной кислоты (или 3 % - ным раствором борной кислоты) и снова водой. Попадание даже очень маленьких кусочков или капель концентрированного раствора едкого натра в глаза может вызвать ожоги с полной потерей зрения. Поэтому необходимо срочно снять кусочки со слизистых глаз (вымыть водой). После удаления кусочков и капель обильно смыть водой, нейтрализовать так же раствором борной кислоты и повторно промыть водой.
Оксид кальция при попадании на кожу вызывает глубокие ожоги (язвы) и тяжелые ожоги глаз. Так как оксид кальция широко растворим в воде, то с кожи его можно удалить растительным или машинным маслом. Глаза промыть водой в течение 10-15 минут и затем 5 % - ным раствором хлорида аммония.
При ожоге соляной кислоты необходимо сразу же (в течение 5-10 минут) промыть пораженное место под сильной струей воды; обработать раствором 3 %-ной соды.
Примечание: во всех случаях поражения глаз щелочами и кислотами необходимо после оказания первой помощи обратиться к врачу – офтальмологу. /6, 7/
Карбонат натрия (кальцинированная сода) представляет собой бесцветные кристаллы с высокой степенью гигроскопичности. Растворимость в воде 16, 69 % по массе, поглощают углекислый газ из воздуха. Растворы имеют сильно щелочную реакцию. Температура плавления + 8530 С.
Гидроксид натрия (едкий натр, каустическая сода) представляет собой белые непрозрачные кристаллы. Сильное основание, которое поглощает углекислый газ и воду из воздуха. Водные растворы имеют сильно щелочную реакцию, температура плавления + 3230 С. ПДК в воздухе – 0,5 мг/м3.
Оксид кальция (негашеная известь) представляет собой гироскопический, белый порошок, состоящий из бесцветных кристаллов. Энергично взаимодействует с водой, образуя гидроксид кальция – гашеную известь. Водные растворы имеют сильнощелочную реакцию. Температура плавления + 26300С.
Все работы с каустической содой и негашеной известью следует проводить в специальной одежде и в защитных очках. /3-5,7,8/
В лабораторной работе используется стеклянная химическая посуда: воронка Бюхнера, колба Бунзена, мензурки, коническая и мерные колбы, цилиндры, фарфоровый стакан и др.; оборудование: водяной термостат, насос Камовского, технические весы. При выполнении лабораторной работы необходимо руководствоваться общими требованиями по охране труда в химической лаборатории./7/
Дополнительно инструкция по технике безопасности к лабораторной работе «Каустификация содового раствора» включает следующие позиции:
1) при приготовлении растворов карбоната натрия, гидроксида кальция растворение вести в условиях охлаждения водой, используя водяную баню или кристаллизатор. Работу проводить в перчатках и защитных очках;
2) экспериментальная часть лабораторной работы проводится в вытяжном шкафу. За 30 минут до начала выполнения опытов необходимо включить вытяжку;
3) перед включением электроприборов проверить заземление мешалки и термостата;
4) отрегулировать работу перемешивающего устройства для обеспечения равномерности перемешивания без разбрызгивания жидкости;
5) взвешивание карбоната натрия и оксида кальция осуществлять в бюксах;
6) каустицер должен быть обязательно термостойким. Для этого используют специальную химическую посуду из стекла или фарфора (рекомендуется в качестве каустицера применять фарфоровый стакан емкостью 1000 мл);
7) отбор проб в реакционной смеси осуществлять с помощью пипетки и резиновой груши. Категорически запрещается засасывать жидкость в пипетку ртом;
8) при титровании негашеной извести в ступке быть предельно аккуратным и внимательным, так как при растирании пестиком комочков извести может произойти выплескивание содержимого;
9) при фильтровании под вакуумом на колбу Бунзена необходимо надеть чехол из тканевого или полиэтиленового материала. Наиболее удобным является чехол из прозрачной клейкой ленты;
10) для снятия воронки Бюхнера необходимо выравнить давление в колбе Бунзена. Для этого левой рукой придерживать колбу, а правой рукой осторожно раскачивать резиновую пробку;
11) по окончании опыта выключить термостат и осторожно вынуть реактор-каустицер;
12) отфильтрованный шлам (мел) утилизировать или смывом большим количеством воды в канализацию или поместить в полиэтиленовый (бумажный) пакет и перенести в ведро для отходов;
13) через 20-30 минут после окончания лабораторной работы выключить вытяжной шкаф;
14) используемую лабораторную посуду после завершения работы необходимо тщательно вымыть сначала проточной водой, а затем ополоснуть дистиллированной водой./1,7/
6. План выполнения лабораторной работы
1. Контроль уровня знаний необходимого для выполнения лабораторной работы.
2. Приготовление химических растворов.
3. Сбор лабораторной установки.
4. Выполнение экспериментальной работы.
5. Обработка экспериментальных данных.
6. Оформление отчета.
7. Защита лабораторной работы.
7. Используемая посуда и оборудование
В лабораторной работе «Каустификация содового раствора» используется химическая посуда и оборудование представленные в табл. 1.
Таблица 1Технические средства, используемые в лабораторной работе
| Наименование технических средств | Основные размеры и параметры | Нормативно-техническая документация | Количество единиц |
| 1 | 2 | 3 | 4 |
| насос Камовского | ТУ 79 РСФСР 277-77 | 1 | |
| колба Бунзена | объем 500 мл | ТУ 92-891.029-91 | 1 |
| колба коническая плоскодонная | объем 250 мл объем 500 мл | ТУ 92-891.029-91 | 2 |
| колба мерная | объем 250 мл | ГОСТ 1770-74 | 1 |
| колба для титрования | объем 100 мл | ГОСТ 1770-74 | 4 |
| чашка Петри | диаметр 7 см | ГОСТ 2536-82 | 1 |
| цилиндр | объем 100 мл объем 500 мл | ГОСТ 1770-74 | 3 |
| воронка лабораторная | диаметр 3 см диаметр 7 см | ГОСТ 2536-82 | 2 |
| ультратермостат | 1 | ||
| технические весы | ВЛ-4М | 1 |
Также в лабораторной работе используются: воронка Бюхнера, часовое стекло, кристаллизатор, градуированная мензурка, стеклянная палочка, бюкс с крышечкой, фарфоровый стакан, фарфоровая ступка с пестиком, шпатель.
8. Используемые реактивы
В лабораторной работе «Каустификация содового раствора» исходными веществами являются кальцинированная сода (карбонат натрия) ГОСТ 83-79 оксид кальция (негашеная известь) ГОСТ 8677-76, дистиллированная вода. Для проведения эксперимента используют 16% раствор карбоната натрия, тонкоизмельченную известь или известковое молоко.
9. Приготовление растворов и проверка их концентрации
9.1 Приготовление 1Н соляной кислоты (HCl) для титрования
Перед приготовлением необходимо определить исходную концентрацию соляной кислоты. В мерный цилиндр объемом 50 мл налить 25-30 мл концентрированной кислоты и измерить ее плотность ( р конц.HСL) с помощью ареометра с интервалом измерения 1,750-1,850. По справочнику определить процентную концентрацию кислоты ( W конц. HCl). Рассчитать объем соляной кислоты (V конц. HCl), необходимый для приготовления 1000 мл 1Н раствора кислоты по формуле 4:
Похожие работы
... в автоклавах, щелочи (для вольфрамита) и кислотами. Это позволяет интенсифицировать автоклавно-содовое разложение вольфрамовых концентратов, сократить расходы соды и в ряде случаев проводить процесс в одну стадию. Последнее увеличивает производительность автоклавов[4]. 4. Получение вольфрамового ангидрида 4.1 Переработка растворов вольфрамата натрия Растворы в, содержащие 60—150 г/л ...
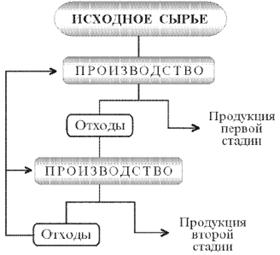
... отходам производства. В докладе «О состоянии окружающей природной среды Российской Федерации в 1997 году» Государственного комитета Российской Федерации по охране окружающей среды отмечается, что на начало 1997 г. на предприятиях различных отраслей промышленности накоплено 1431,7 млн. т токсичных отходов. За 1997 г. на промышленных предприятиях РФ образовалось 89,4 млн т токсичных отходов, из ...






0 комментариев