Навигация
Расчет кривой титрования методом комплексонометрии
2.3 Расчет кривой титрования методом комплексонометрии
Оценить возможность титриметрического определения и построить кривую титрования для следующих данных 0,05М ZnCl2 0,025M Na2H2Y, pH 9, концентрация аммиака 0,1 моль/л.
Запишем уравнение титриметрической реакции:
Zn2++ H2Y2-→ZnY2-+2H+
Расчет кривой титрования сводится к расчету показательной концентрации Zn2+ в зависимости от объема титранта. Устойчивость ZnY2- зависит от кислотности среды (чем выше кислотность, тем ниже устойчивость), в связи с этим для связывания ионов водорода, количественное определение ZnCl2 проводят в среде аммонийного буфера.
Рассчитаем объем титранта по закону эквивалентов:
![]() (1)
(1)
откуда
 (2)
(2)

Наличие иона Н+ в среде, где присутствует трилон В, приводит к протеканию следующих конкурирующих реакций:
Y4-+H+ « HY3-, ![]() = K4;
= K4;
HY3-+H+ « H2Y2-, ![]() = K3;
= K3;
H2Y2-+H+ « H3Y-, ![]() = K2;
= K2;
H3Y-+H+ « H4Y, ![]() = K1;
= K1;
где K1, K2, K3, K4 – константы ступенчатой диссоциации H4Y (K1=1,0.10-2, K2=2,1.10-3, K3=6,9.10-7, K4=5,5.10-11)[5].
Рассчитаем условную константу устойчивости, которая выражает прочность комплексов цинка с трилоном В:
 (3)
(3)
![]()
Рассчитаем коэффициенты конкурирующих реакций:
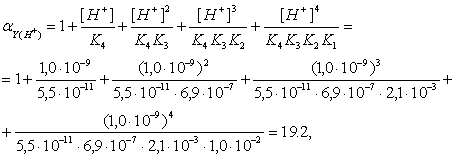 (4)
(4)
Zn2+ участвует также в конкурирующих реакциях образования комплексных соединений с аммиаком NH3 в соответствии со следующими уравнениями реакций:
n2++NH3![]() Zn(NH3)2+,
Zn(NH3)2+,
Zn2++2NH3![]() Zn(NH3)22+,
Zn(NH3)22+,
Zn2++3NH3![]() Zn(NH3)32+,
Zn(NH3)32+,
Zn2++4NH3![]() Zn(NH3)42+,
Zn(NH3)42+,
![]() (5)
(5)
По данным литературного источника[5]


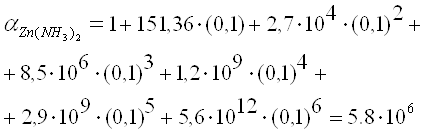
Подставив, выражения (4) и (5) в уравнение константы устойчивости (3) получим:

1) до начала титрования, в отсутствии конкурирующих реакций с участием цинка, концентрация ионов Zn2+ равна концентрации соли ZnCl2
ZnCl2 →Zn2++2Cl-
[Zn2+]=C![]() =0.05 моль/л
=0.05 моль/л
2)до точки эквивалентности величина pZn определяется концентрацией неоттитрованного иона цинка уравнение (а), так диссоциацией комплексоната, образующегося по уравнению(б) при избытке ионов цинка можно пренебречь.
а)Zn2++H2Y2-→ ZnY2-+2H+
б)ZnY2- ↔Zn2++Y4-.
![]() дис.
дис.
![]() (6)
(6)
Проведем расчет для точек ![]()
3) В точке эквивалентности расчет концентрации ионов Zn2+ проводится с учетом уравнения реакции диссоциации комплекса:
ZnY2-↔Zn2++Y4-
Данное равновесие количественно описывается константой:
 (7)
(7)
[Zn2+] = [Y4-] = x,
[ZnY2-] = [ZnCl2],
![]() ,
,
 ,
,
![]() ,
,
[Zn2+] = 1,8 ∙ 10-5
pZn = 4.7
4)после точки эквивалентности концентрация комплексоната металла остается постоянной
Концентрация ионов лиганда определяется избытком добавленного титранта:
 (8)
(8)
 (9)
(9)
откуда :

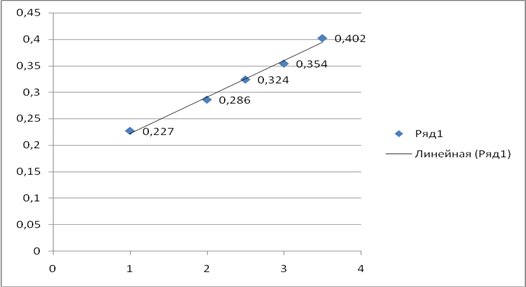
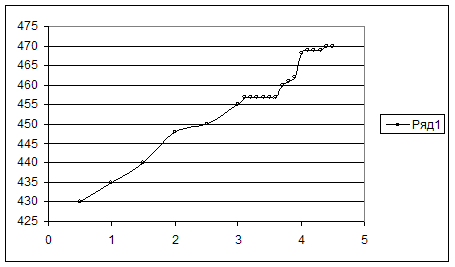
Для найденных значений [Zn2] и [Y4-] вычисляются значения pZn2+ и pY4- и строится кривая титрования в координатах pZn2+- Vтитранта. Проводится анализ кривой титрования, рассчитывается скачок титрования, выбирается индикатор.
В таблице 3 представлены данные расчета изменений концентрации ионов определяемого вещества и титранта в зависимости от объема добавляемого титранта (при условии что объем раствора в процессе титрования не изменяется).
Таблица 3-Изменение pZn при титровании трилоном Б.
| Ŋ | VТ,мл | [Y4-] | pY4- | [Zn2] | pZn2+ |
| 0 | 0 | - | - | 0.05 | 1.3 |
| 0.1 | 20 | - | - | 0.025 | 1.6 |
| 0.2 | 40 | - | - | 0.02 | 1.7 |
| 0,4 | 80 | - | - | 0.015 | 1,8 |
| 0.8 | 160 | - | - | 0.005 | 2.3 |
| 0.9 | 180 | - | - | 0.0025 | 2.6 |
| 0.99 | 198 | - | - | 0.00025 | 3.6 |
| 0.999 | 199.8 | - | - | 0.000025 | 4.6 |
| 1 | 200 | - | - | 1.8.·10-5 | 4.7 |
| 1.001 | 200.2 | 5·10-5 | 4.3 | 3.125·10-6 | 5.5 |
| 1.01 | 202 | 5·10-4 | 3.3 | 3.12·10-7 | 6.5 |
| 1.05 | 210 | 2.5·10-3 | 2.6 | 6.2·10-8 | 7.2 |
| 1.1 | 220 | 5·10-3 | 2.3 | 3.1·10-8 | 7.5 |
| 1.2 | 240 | 0.01 | 2 | 1.5·10-8 | 7.8 |
| 1.8 | 360 | 0.04 | 1.4 | 3·10-9 | 8.4 |
| 2 | 400 | 0.05 | 1.3 | 3.12·10-9 | 8.5 |
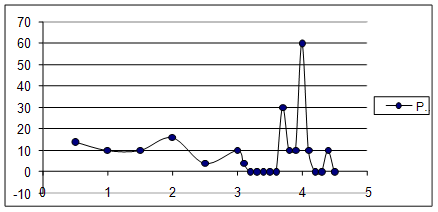
Проанализируем полученную кривую. Как видно, в области точки эквивалентности происходит резкое изменение концентрации ионов цинка, которое можно отметить с помощью соответствующего индикатора. Скачок титрования составляет pZn2+=6.5-3,6=2,9, то есть величину достаточную для фиксирования точки эквивалентности. На основании этого можно сделать вывод о возможности комплексонометрического определения цинка в области заданных концентраций.
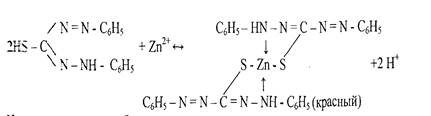
Индикаторами в комплексонометрии являются металлоидикаторы , образующие с ионами металлов интенсивно окрашенные соединения, константы устойчивости которых, однако, ниже чем константы бесцветных комплексов трилона Б с ионами металлов [3].
Подбор индикатора осуществляется в соответствии с условиями титрования, описанными в справочнике Лурье [5]. Сопоставив условия титрования, представленные в задаче, с данными из справочника [5], приходим к заключению что, в данном случае индикатором является 0,1% водный раствор кислотный хром синий К, обеспечивающий переход окраски из розовой в серо-голубую.
Похожие работы
... и синей, подобны свойствам фосфорномолибденовых гетерополикомплексов. Поэтому основная трудность при определении мышьяка этим методом заключается в отделении мышьяка от фосфора [7]. 2.2.2.1 Количественное определение мышьяка в неизвестном минерале Навеску металла разрушают азотной кислотой, сурьмяную кислоту связывают тартратом и мышьяк выделяют вместе с магний-аммоний фосфатом. После чего ...
... состоит анализируемое вещество и какие ионы, группы атомов или молекулы входят в его состав. При исследовании состава неизвестного вещества качественный анализ всегда предшествует количественному, так как выбор метода количественного определения составных частей анализируемого вещества зависит от данных, полученных при его качественном анализе. Качественный химический анализ большей частью ...
... по типам веществ. Во втором случае, когда времена удерживания известных соединений и зон образца не совпадают, имеется возможность предсказать время удерживания неизвестного компонента. Вполне надежны предсказания относительного удерживания на основании данных о структуре в пространственно-эксклюзионной хроматографии. Менее точны они в адсорбционной, распределительной хроматографии и особенно ...
... (II) аммония. Cd2+-+ [Hg(SCN)4]2- -> Cd[Hg(SCN)4] ()бразование бесцветных продолговатых кристаллов тетрароданомеркурата кадмия Аналитически реакции катионов VI аналитической группы по кислотно-основной классификации: Cu2+, Hg2+, Cd2+, Co2+, Ni2+ Групповой реагент – NH4OH в избытке Хотя элементы расположены в разных груупах периодической системы Д.Ию Менделеева, все эти катионы ...


0 комментариев